
У нас целый мир гомеопатии. Лечение гомеопатией в Одессе, ул. Тираспольская, 13 Центральная Одесская гомеопатическая аптека (аптека №5 ОАО "Фармация"). У нас Вы найдете все гомеопатические препараты. Узнаете о классической гомеопатии и все о последних форумах и семинарах по гомеопатии.

|
Поиск:
Гомеопатия - это...
Карта сайта
Написать письмо врачам
Написать письмо в аптеку
Правила записи на консультации врачей
Публикации по гомеопатии
Materia Medica динамизированных лекарственных препаратов...
История и практика использования биотерапевтических средств...
Гомеопатические средства в неврологии и медицинской реабилитации...
Препараты из насекомых...
Периодические профессиональные издания
Международные новости
Семинары, конференции, форумы
Одесские Гомеопатические Конгрессы
И снова о фаршированной рыбе
Объявления для гомеопатов
События, даты, поздравления и комментарии
Книги и журналы для гомеопатов
Новые издания по гомеопатии
Одесское гомеопатическое общество
Анкеты консультантов и лекторов Общества
Одесская гомеопатическая аптека
История аптеки
Номенклатура динамизированных средств
Монокомпонентные средства
Сверхвысокие разведения ГЛС
Многокомпонентные динамизированные средства
Изготовление гомеопатических лекарств
История гомеопатии в регионе
Materia medica
Гомеопатия для чайников
Вопрос - ответ
Дружественные сайты
|
Results of multitarget anti-PD-1 / PD-L1 / CD19 / CD25 / CD38 therapies with use of Mercurid drugs in patients with different oncopathology. A.V. Artemov, E.S. Buryachkovsky, A.V. Lukyanchuk, S.N. Gusev (Odessa, Ukraine) The study of the functioning of the immune system in the occurrence and development of malignant neoplasms is of great practical interest. Since, despite the successes of modern cancer immunotherapy with the use of Immune Checkpoint Inhibitors molecules, they demonstrate limited efficacy of up 10 to 20%, which is not enough given their cost from $156,000 to $257,000. According to the authors of the study, it is possible to increase the effectiveness of immunotherapy and make it available to millions of patients. For this purpose, the innovative homeopathic preparation Mercuryd was created. Its molecules are a modulator of activity of 4 target proteins PD-1/PD-L1, CD19, CD25, CD38. That predetermines greater efficiency in comparison with preparations inhibitors of only one target protein PD1 or PD-L1. Ключевые слова: Меркурид, мультитаргетная терапия, рак
Ключовi слова: Меркурiд, мультитаргетна терапiя, рак
Key words: Mercurid, multitarget therapy, cancer
Иммунные контрольные точки для лечения рака
Опухолевые клетки способны избежать контроля и разрушения иммунной системой, используя ряд сложных и часто перекрывающихся механизмов, которые приводят к нарушению ключевых компонентов, участвующих в эффективном противоопухолевом ответе (J.Swann, M.Smyth, 2007). Раковые клетки, чтобы избежать атаки со стороны иммунной системы используют иммунные контрольные точки (Immune checkpoint), чтобы выжить. На поверхности трансформированных клеток появляются особые белки (PD-L1), которые при контакте с рецептором клетки-киллера (лимфоцитом) сообщают ему, что они «не раковые». Лимфоцит, получив такой сигнал не атакует опухоль, впадает в состояние анергии. В этом случае, раковые клетки могут выживать в организме пациента.
Путь PD-1/PD-L1
Рецептор PD-1 (англ. Programmed cell death 1; CD279) экспрессируется на поверхности активированных Т-клеток. Его лиганды, PD-L1 (B7-H1, CD274) и PD-L2 (B7-DC, CD273) обычно экспрессируются на поверхности дендритных клеток или макрофагов. PD1 и PD-L1/PD-L2 относятся к семейству иммунных контрольных белков, которые действуют как коингибирующие факторы, которые могут остановить развитие ответа Т-клеток. В физиологическом плане, путь PD1/PD-L1 гарантирует, что иммунная система активируется только в соответствующее время, чтобы свести к минимуму возможность хронического аутоиммунного воспаления.
Таким образом, PD-L1/PD-L2 расположены не только на опухолевых клетках, но и на дендритных клетках и макрофагах – выполняя важную функцию иммунологической толерантности.
Врачи и пациенты, уже столкнулись с ситуацией, когда на фоне anti-PD-L1/PD-L2 терапии у пациентов развился СД-1 типа (Yale University, immunologist Kevan Herold) или произошло аутоиммунное повреждение структур сердца, вызвавшее смерть пациентов (autoimmune attacks on the heart, called lymphocytic myocarditis, Andrew Lichtman, a pathologist at Brigham and Women’s Hospital in Boston).
Обзор anti-PD-1/PD-L1 терапии
В течение последних 2 лет ингибиторы анти-PD-1, ниволумаб (OPDIVO, Bristol-Myers Squibb) и пембролизумаб (KEYTRUDA, Merck Sharp и Dohme Corporation) и ингибитор анти-PD-L1 атезолизумаб (TECENTRIQ, Genentech Oncology) были одобрены Управлением по контролю за продуктами и лекарствами США (FDA) в лечении пациентов с продвинутым НМРЛ с прогрессированием при терапии первой линии или после нее. Европейское агентство по лекарственным средствам (EMA) одобрило Nivolumab и Pembrolizumab по тем же признакам. Эти препараты на основе моноклональных антител (англ., MAbs) формируют ТОП-6 продаж мировой фармы. Но, при всех их коммерческой привлекательности, они демонстрируют ограниченную эффективность от до 10 до 20%, что недостаточно учитывая их стоимость от $156000 до $257000 курс (Xiaohui Wang et al., 2017; Hashem O. Alsaab et al., 2017).
Кроме того, несмотря на клинический успех иммунотерапии против PD-1/PD-L1, часть пациентов не реагирует на эти методы лечения (Philips и Atkins, 2014; Tumeh et al., 2014).
Молекулы Меркурида для повышения эффективности анти-PD-1/PD-L1 терапии
Хотя исследования указывают на необходимость терапии иммунных контрольных точек (Immune checkpoint), однако в практике её сдерживает высокая стоимость брендовых препаратов, риск развития побочных эффектов и ограниченная эффективность, обусловленная действием препаратов только на один белок-мишень.
Альтернативой этим препаратам может стать отечественный инновационный гомеопатический препарат Меркурид (РС МОЗ №UA6098/01/01), который является модулятором активности 4 белков мишеней PD-1/PD-L1, CD19, CD25, CD38. Действующее вещество Меркурида – инновационные молекулы MSC-428 (Патенты Украины, России, Белоруссии, США). Которые являются низкомолекулярным координационным комплексом хелатного типа, в котором центральный атом металла связан с молекулами L-цистеина. При молекулярной массе 440 Da размер молекулы составляет 1,2 нм.
Ноу-хау (от англ. know how — знать как) разработчиков новой молекулы, является сверхмалый размер молекул, который позволяет встраиваться в активный сайт связывания рецептора клетки, а наличие атома металла, предопределяет конформационные изменения в пространственной структуре белка-рецептора. В результате этого утрачивается комплементарность - соответствие между лигандами и рецепторами, относящимися к суперсемейству иммуноглобулинов. Таким образом, несмотря на различия в аминокислотной последовательности рецепторов PD-1/PD-L1, CD19, CD25, CD38 их объединяет наличие трехмерной структуры необходимой для специфического распознавания своего лиганда (Voet Donald, Biochemistry. 2 edition John Wiley&Sons; 1995). Уникальность этой структуры определяется дисульфидными (?S?S?) связями молекул цистеина (Wang Xinquan et. al., 2009).
Молекулы MSC-428 разрывают дисульфидные связи (?S?S?) в рецепторе, а ион металла вызывает конформационную перестройку трехмерной структуры рецептора, нарушая тем самым комплементарность, т.е. пространственное соответствие рецептора своему лиганду (Alexey V. Onufriev and Emil Alexov, 2015). В результате, рецептор не способен присоединить лиганд и деструктивные сигналы в клетку, не поступают (Boehr David D., et. al., Science 2008). Таким образом, молекулы MSC-428 осуществляют мультитаргетную терапию, направленною против четырех белков мишеней - PD-1/PD-L1, CD19, CD25, CD38, что предопределяет большую эффективность по сравнению с традиционной терапией иммунных контрольных точек, где ингибируется только один белок мишень.
Цель и задачи исследования
1. В сравнительном исследовании охарактеризовать особенности функционального состояния Т- и В-лимфоцитов крови у больных раком легкого, раком желудка, раком молочной железы, колоректальным раком.
2. Изучить фенотипы лимфоцитов крови по экспрессии дифференцировочных CD3, CD4, CD8, CD16, CD19 и активационных маркеров CD25, CD38, CD45, CD54, CD95 у больных раком легкого, раком желудка, раком молочной железы, колоректальным раком.
3. Оценить фенотипические сдвиги в лимфоцитах онкологических больных в зависимости от течения и исхода заболевания.
Объем исследования
В исследовании принимали участие 530 пациентов, которые были распределены на 3 группы.
Группу Меркурид составили 192 больных, ранее пролеченных разными комбинациями противоопухолевых препаратов. Эти пациенты получали Меркурид в качестве единственно возможной терапии после того, как возможности стандартной ХТ были исчерпаны. Возраст больных находился в пределах от 28 до 74 лет, средний возраст — 56,5 лет. Мужчин — 72, женщин — 120 человек. У 57 пациентов в прошлом проводилась лучевая терапия. Общее состояние больных по критериям Всемирной организации здравоохранения (ВОЗ) в среднем оценивалось как 2,9. Продолжительность приема препарата составила 2 мес. Анализы проводили в 1 день и 60 день приема препарата.
Группа Меркурид + ХТ, составили 174 пациента. Возрастом от 29 до 75 лет. Средний возраст — 50,1 лет. Мужчин — 68, женщин — 106 человек. Все больные страдали распространенной стадией онкологического заболевания и ранее получили от 2 до 19 курсов ХТ, у 52 пациентов проводилась лучевая терапия. Общее состояние больных по критериям Всемирной организации здравоохранения (ВОЗ) в среднем оценивалось как 2,6. Пациенты принимали Меркурид в течении 2 мес, в перерывах между курсами ХТ и ЛТ. Забор крови проводился вначале и по окончанию приема Меркурида.
Группа контроль — 164 пациента. Возраст от 32 до 81 года. Средний возраст — 54 года. Все пациенты получали от 4 до 21 курса ХТ согласно своему диагнозу и протокола терапии. 62 пациента проходили лучевую терапию. Эти пациенты не получали иммунотропной терапии. Общее состояние больных по критериям Всемирной организации здравоохранения (ВОЗ) в среднем оценивалось как 2,8. С целью оценки способности восстановления собственных механизмов адаптации, анализы проводили дважды, вначале и спустя 2 мес.
Действие нового препарата избирательно направлено на имеющиеся генетические/биохимические изменения в иммунном статусе пациентов. Это отвечает современным тенденциям в медицине, где намечается переход от лечения нозологической формы опухоли к лечению фенотипических и генетических изменений в иммунной системе больного, так называемое направление Precision Oncology (досл., Точная онкология).
Таблица 1. Характеристика больных включённых в исследовании
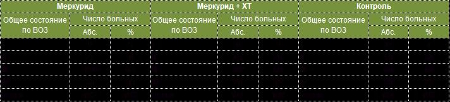
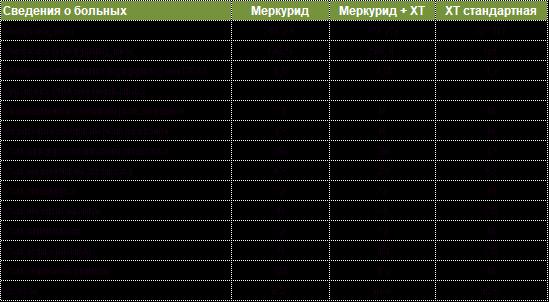
Иммунологические исследования
Основу патогенеза злокачественных опухолей составляют иммунологические нарушения, которые наряду с повреждением генетического аппарата клеток, проявляются дисфункцией клеточного звена иммунной системы, искажением механизмов контроля и дифференцировки клеток, иммунологической толерантностью и невозможностью эффективного иммунного ответа на развивающуюся опухоль (Антонов В.Г., Козлов В.К., 2004; Заридзе Д.Г., 2004; Tubiana M., 2008; Finn O.J., 2008; Prendergast G.C., 2008).
1. Динамика изменения количества лимфоцитов с фенотипом CD16 (NK-клетки)
Важным элементом противоопухолевой защиты являются естественные клетки-убийцы, сокращённо – NK-клетки (от англ. nature kller). Особенностью действия NK-клеток является то, что они уничтожают клетки, на которых снижена экспрессия молекул HLA I класса, что характерно для опухолевых клеток.
В группе Меркурид, восстановление экспрессии CD16 произошло у 61% пациентов. Группа Меркурид+ХТ – 63%. В контрольной группе, незначительное восстановление экспрессии CD16 на уровне +3%, по сравнению с началом исследования.
Таблица 1. Пациенты у которых восстановилась до нормы CD16 клетки, %
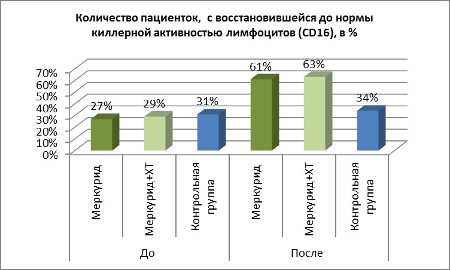
2. Динамика изменения количества лимфоцитов с фенотипом CD25, CD95
Повышенная готовность клетки к апоптозу сопровождается экспрессией мембранного гликозилированного белка АРО-1/Fas (Fas-рецептора, Fas-R), взаимодействие которого со специфическим лигандом (Fas-L) инициирует процесс апоптотической гибели (Trauth B.C. et al., 1989; Yonehara S. et al., 1989; Nagata S., Golshtein P., 1995).
Исследования последних лет показывают, что прием химиопрепаратов, применяемых в онкотерапии сопровождается изменением экспрессии CD95 и сопряжены с аномальным апоптозом иммуноцитов.
В исследовании большинство пациентов (82%) имели повышенную экспрессию Fas- рецептора CD95+ и сниженную к IL-2 (CD25), что способствовало апоптической гибели активированных лимфоцитов и развитию лимфопении.
Молекулы MSC-428 являются агонистами CD25 и антагонистами CD95.
В группе, принимавшей Меркурид отмечено его влияние на повышение экспрессии лимфоцитов с фенотипом CD25+ и снижением CD95+, что коррелирует с увеличением выработки IL-2, цитокина, который повышает цитолитическую функцию Т-киллеров и NK-клеток, увеличивает продукцию этими клетками перфоринов и интерферона-гамма.
Меркурид увеличивает выработку IL-2, что способствует увеличению экспрессии MHC I класса, улучшая распознаваемость антигенов опухоли.
В группе Меркурид терапевтический ответ – 64%. Меркурид+ХТ – 61%. В группе контроля, восстановление у 24%.
Таблица 2. Динамика изменения лимфоцитов CD25, CD95

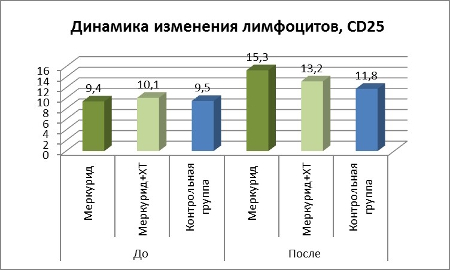
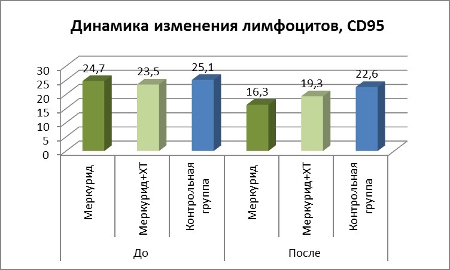
3. Динамика изменения количества лимфоцитов с фенотипом CD38
CD38 кодирует мембранный белок, участвующий в адгезии клеток и катализирующий образование циклической АDP-рибозы. Показано, что в опухолевых очагах больных присутствуют клетки, в которых происходит устойчивая экспрессия CD38. Высокий уровень экспрессии CD38 ассоциировался с необходимостью раннего начала химиотерапии и меньшей общей выживаемостью даже у пациентов на ранних стадиях заболевания (Rodrigo Santacruz, Neus Villamor, Haematologica. 2014).
CD38 повышается при карциноме молочной железы, начиная со второй стадии опухолевого роста и сохраняется повышенным на последующих стадиях вне зависимости от местоположения очагов метастазирования. Наиболее высокое содержание исследуемого антигена наблюдается при комбинированной гистологической форме опухоли, статистически достоверно повышенные уровни CD38 сохраняются как при наличии единичных, так и множественных очагов поражения. Высокая концентрация CD38 антигена характерна для опухолей любого диаметра (Liao S, Xiao S, Oncol Rep. 2014)
Существует модель участия CD38 антигена в ограничении процессов миграции мононуклеарных клеток из сосудистого русла в тканевое пространство, а соответственно к месту локализации опухоли. Таким образом, повышенный уровень CD38 антигена можно рассматривать в качестве одного из факторов ухода опухоли от противоопухолевого ответа со стороны иммунной системы и развития неотвечаемости лимфоцитов на опухолевые антигены и нарушение механизма иммунных контрольных точек PD-1/PD-L1.
Нормализация CD38 происходит на фоне ремиссии, таким образом, целесообразно использовать его в качестве мониторингового прогностического показателя при терапии карциномы молочной железы. Молекулы MSC-428 антагонисты CD38.
Таблица 3. Динамика изменения лимфоцитов CD38
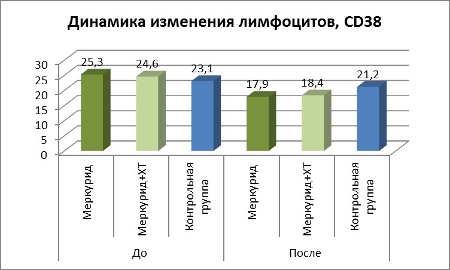
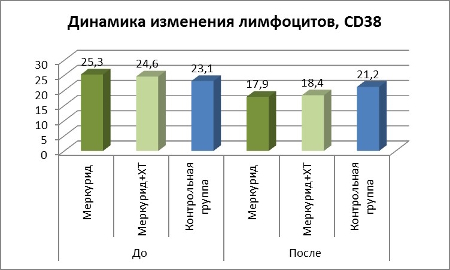
Изменение уровня экспрессии и активности CD38 является адекватным показателем интенсивности патологического процесса и эффективности проводимой терапии.
В группе Меркурид, произошло более выраженное снижение экспрессии CD38 – 70% пациентов. В группе Меркурид + ХТ, на терапию отреагировало – 64%. В контрольной группе уменьшение CD38 отмечено только у 9% пациентов.
4. Динамика изменения количества лимфоцитов с фенотипом CD19
CD19 это мембранный антиген B-клеток. Принадлежит к суперсемейству иммуноглобулинов. Играют двоякую роль в противоопухолевой защите.
В случае гиперактивации, секретируют иммуноглобулины (антитела), которые связываются с антигенами опухоли. Но опухолевая клетка имеет особенность: она может терять свои поверхностные антигены. Фоновый уровень комплемента у человека недостаточен для развития антителозависимого лизиса опухолевой клетки. Комплекс антиген-антитело покидает опухолевую клетку раньше, чем происходит активация и полимеризация комплемента. Образующиеся антитела и циркулирующие иммунные комплексы блокируют антигены опухолевых клеток и рецепторы Т-киллеров, защищая опухолевую клетку от Т-лимфоцитов киллеров.
В случае недостаточности В-лимфоцитов, они не вырабатывают в достаточном количестве IgM, необходимый для комплементзависимого лизиса опухолевых клеток
Молекулы MSC-428 являются смешанными агонистами-антагонистами CD19.
При исследовании установлен различные изменения в экспрессии В-клеток. В группе Меркурид, на начало исследования, нормальный уровень В-лимфоцитов с маркером CD19 был у 35%. Восстановление до нормы произошло у 71% пациентов.
В группе Меркурид + ХТ первоначально этот показатель был в норме у 31% пациентов. Вероятно, это связано с последствиями химиотерапии, которая оказала негативное влияние на систему гуморального иммунитета. Терапевтический ответ – 68%
В группе контроля уровень CD19 клеток был в норме у 29% пациентов. За период наблюдения оставался практически на том же уровне. Что также могло быть связано с курсами проводимой ХТ. Восстановился до нормы у 32% (+3%).
Таблица 4. Количество пациентов, у которых восстановилась до нормы CD19, в %.

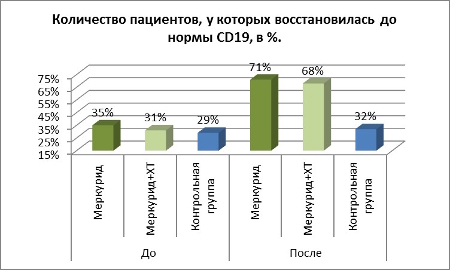
Выводы
Предлагаемая стратегия улучшения терапии против PD-1/PD-L-1 при помощи лекарственного препарата Меркурид расширяет возможности терапии иммунных контрольных точек (Immune checkpoint). Патентованные молекулы «MSC-428» гомеопатического препарата Меркурид:
1. «MSC-428» вызывает конформационные изменение в 3-х мерной конформации рецепторных белков PD-1, что препятствует их связыванию с PD-L1 опухоли
2. «MSC-428» увеличивает экспрессию CD25 Т-клеток, нормализует выработку IL-2, что повышает способность T-киллеров убивать опухолевые клетки и стимулирует выработку перфоринов и гранзимов.
3. «MSC-428» снижает повышенную активность CD19, которые экранируют опухолевые антигены и препятствуют атаки цитотоксических Т-клеток.
4. Молекула «MSC-428» ингибирует киназу ZAP-70, уменьшает избыточную экспрессию CD38, что повышает противоопухолевые реакции организма и мобилизует цитотоксический потенциал CD8, CD16 Т-лимфоцитов, препятствует развитию резистентности к опухолевым клеткам.
Применение Меркурида в таргетной иммунотерапии обеспечивает формирование эффективного противоопухолевого ответа пациента. Действие молекул направлены на 4 белка мишени, такие как PD-1/PD-L1, CD19, CD25, CD38. Необходимо отметить, что восстановление их активности, во многом предопределило нормализацию других поверхностных антигенов лимфоцитов, таких как CD3, CD4, CD8, CD16, CD45, CD95, систему фагоцитоза, выработку иммуноглобулинов класса A,M,G.
По нашему мнению, только комплексное воздействие обеспечивает построение целостной, эффективной и безопасной стратегии иммунотерапии пациентов.
Применение препарата в иммунотерапии пациентов с онкопатологиями:
• Препятствует апоптической гибели иммуноцитов, индуцированной как опухолью, так и последствия специального лечения
• Нормализует число лимфоцитов с фенотипом CD3, CD4, CD8
• Увеличивает киллерную активность NK-клеток (CD16), CD8
• Снижает гиперактивность провоспалительных цитокинов
• Восстанавливает систему фагоцитоза, скомпрометированную ХТ и ЛТ
• Уменьшает экспрессию CD38, предотвращая эффект иммунной неотвечаемости на опухолевые антигены
• Понижает экспрессию CD54 (ICAM-1), препятствуя ангиогенезу опухоли
• Оказывает комплексное действие на PD-1/PD-L1/CD19/CD25/CD38, что более эффективно увеличивает способность иммунной системы пациентов лизировать опухолевые клетки.
1. Блохин Д.Ю. Программированная гибель клеток в механизмах циторедуктивной терапии опухолевых заболеваний: В кн. «Клиническая онкогематология» под ред. проф. М.А. Волковой. – М.: Медицина, 2007. – С.200–16.
2. Герасимова Г.К. Механизм действия противоопухолевых препаратов. – С.217–45.
3. Belani C.P. The role of irreversible EGFR inhibitors in the treatment of non-small cell lung cancer: overcoming resistance to reversible EGFR inhibitors // Cancer Invest. – 2010. – 28(4). – Р. 413–23.
4. Birchmeier C., Birchmeier W., Gherardi E., Vande Woude G.F. Met, metastasis, motility and more // Nat Rev Mol Cell Biol. – 2003. – 4. – Р. 915–25.
5. Bradley D.A., Daignault S., Ryan CJ. et al. Cilengitide in asymptomatic metastatic castration resistant prostate cancer patients: a randomized phase II trial by the prostate cancer clinical trials consortium // Invest New Drugs. – 2010 March 25.
6. Bukowski R.M. Pazopanib: a multikinase inhibitor with activity in advanced renal cell carcinoma // Expert Rev Anticancer Ther. – 2010. – 10(5). – Р. 635–45.
7. Carpenter G., Cohen S. Epidermal growth factor // J Biol Chem. – 1990. – 265. – Р. 7709–12.
8. Ching L.M., Cao Z., Kieda C. et al. Induction of endothelial cell apoptosis by the antivascular agent 5,6-Dimethylxanthenone-4-acetic acid // Br J Cancer – 2002. – 86. – Р. 1937–42.
9. Davis I.J., McFadden A.W., Zhang Y. et al. Identification of the receptor tyrosine kinase c-Met and its ligand, hepatocyte growth factor, as therapeutic targets in clear cell sarcoma //Cancer Res. – 2010. – 70(2). – Р. 639–45.
10. Dharmawardana P.G., Giubellino A., Bottaro D.P. Hereditary papillary renal carcinoma type I // Curr Mol Med. – 2004. – 4. – Р. 855–68.
11. Fesik S.W. Promoting apoptosis as a strategy for cancer drug discovery//Nat Rev Cancer. – 2005. – 5. – Р. 876–85.
12. Folkman J. Tumor angiogenesis: therapeutic implications // N Engl J Med. – 1971. – 285. – Р. 1182–6.
13. Giaccone G., Zatloukal P., Roubec J. et al. Multicenter phase II trial of YM155, a small-molecule suppressor of survivin, in patients with advanced, refractory, non-small-cell lung cancer // J Clin Oncol. – 2009. – 27(27). – Р. 4481–6.
14. Gridelli C., Rossi A., Bareschino M.A. et al. The potential role of insulin-like growth factor receptor inhibitors in the treatment of advanced non-small cell lung cancer // Expert Opin Investig Drugs. – 2010. – 19(5). – Р. 631–9.
15. Hanahan D., Weinberg R.A. The hallmarks of cancer // Cell. – 2000. – 100. – P. 57–70.
16. Head M., Jameson M.B. The development of the tumor vascular-disrupting agent ASA404 (vadimezan, DMXAA): current status and future opportunities // Expert Opin Investig Drugs. – 2010. – 19(2). – Р. 295–304.
17. Hersey P., Sosman J., O'Day S. et al. A randomized phase 2 study of etaracizumab, a monoclonal antibody against integrin alpha(v)beta(3), + or – dacarbazine in patients with stage IV metastatic melanoma // Cancer – 2010. – 116(6). – Р. 1526–34.
18. Hewish M., Chau I., Cunningham D. Insulin-like growth factor 1 receptor targeted therapeutics: novel compounds and novel treatment strategies for cancer medicine // Recent Pat Anticancer Drug Discov. – 2009. – 4(1). – Р. 54–72.
19. Hinnen P., Eskens F.A. Vascular disrupting agents in clinical development // Br J Cancer. – 2007. – 96. – Р. 1159–65.
20. Hsu J.Y., Wakelee H.A. Monoclonal antibodies targeting vascular endothelial growth factor: current status and future challenges in cancer therapy // BioDrugs. – 2009. – 23(5). – Р. 289–304.
21. Hunter A.M., LaCasse E.C., Korneluk R.G. The inhibitors of apoptosis (IAPs) as cancer targets//Apoptosis. – 2007. – 12. – Р. 1543–68.
22. Jin H., Varner J. Integrins: roles in cancer development and as treatment targets // Br J Cancer. – 2004. – 90. – Р. 561–5.
23. Karp D.D., Paz-Ares L.G., Novello S. et al. High activity of the anti-IGF-IR antibody CP-751,871 in combination with paclitaxel and carboplatin in squamous NSCLC [abstract] // J Clin Oncol. – 2008. – 26(suppl). – Р. 8015.
24. Llovet J.M., Ricci S., Mazzaferro V. et al. Sorafenib in advanced hepatocellular carcinoma // N Engl. J Med. – 2008. – 359. – P. 378–90.
25. McKeage M.J., Reck M., Jameson M.B. et al. Phase II study of ASA404 (vadimezan, 5,6-
dimethylxanthenone-4-acetic acid/DMXAA) 1800mg/m(2) combined with carboplatin and paclitaxel in previously untreated advanced non-small cell lung cancer // Lung Cancer - 2009. - 65(2). - Р. 192–7.
26. Minkovsky N., Berezov A. BIBW-2992, a dual receptor tyrosine kinase inhibitor for the treatment of solid tumors // Curr Opin Investig Drugs. – 2008. – 9(12). – Р. 1336–46.
27. Moroney J.W., Sood A.K., Coleman R.L. Aflibercept in epithelial ovarian carcinoma // Future Oncol. – 2009. – 5(5). – Р. 591–600.
28. Nachmias B., Ashhab Y., Ben-Yehuda D. The inhibitor of apoptosis protein family (IAPs): an emerging therapeutic target in cancer // Semin Cancer Biol. – 2004. – 14. – Р. 231–43.
29. O'Brien S., Moore J.O., Boyd T.E. et al. 5-year survival in patients with relapsed or refractory chronic lymphocytic leukemia in a randomized, phase III trial of fludarabine plus cyclophosphamide with or without oblimersen // J Clin Oncol. – 2009. – 27(31). – Р. 5208–12.
30. Paik P.K., Rudin C.M., Brown A. et al. A phase I study of obatoclax mesylate, a Bcl-2 antagonist, plus topotecan in solid tumor malignancies // Cancer Chemother Pharmacol. – 2010 31. Paik S., Shak S., Tang G. et al. A multigene assay to predict recurrence of tamoxifen treated, node-negative breast cancer // N Engl J Med. – 2004. – 351. – Р. 2817–26.
31. Pollak M. Insulin-like growth factor-related signaling and cancer development // Recent Results Cancer Res. – 2007. – 174. – Р. 49–53.
Результаты мультитаргетной anti-PD-1/PD-L1/CD19/CD25/CD38 терапии с применением препарата «Меркурид» у пациентов с разными онкопатологиями. А.В. Артемов, Э.С. Бурячковский, А.В. Лукьянчук, С.Н. Гусев (Одесса, Украина)
Изучение функционирования иммунной системы при возникновении и развитии злокачественных новообразований представляет большой практический интерес. Поскольку, несмотря на успехи современной иммунотерапии рака с применением молекул ингибиторов иммунных точек (Immune Checkpoint Inhibitors), они демонстрирует ограниченную эффективность (от 10 до 20%), что недостаточно, учитывая их стоимость от $ 156000 до $ 257000 на курс. По мнению авторов исследования, есть возможность повысить эффективность иммунотерапии и сделать ее доступной для миллионов пациентов. Для этого создан инновационный гомеопатический препарат Меркурид, молекулы которого являются модулятором активности 4 белков-мишеней PD-1 / PD-L1, CD19, CD25, CD38. Что обусловливает большую эффективность по сравнению с препаратами-ингибиторами только 1 белка-мишени PD1 или PD-L1.
Результати мультитаргетної anti-PD-1/PD-L1/CD19/CD25/CD38 терапiї з вживанням препарату “Меркурiд” у пацiєнтiв з рiзними онкопатологiями. О.В. Артьомов, Е.С. Бурячковський, О.В. Лукьянчук, С.М. Гусєв (Одеса, Україна)
Вивчення функціонування імунної системи при виникненні і розвитку злоякісних новоутворень становить великий практичний інтерес. Оскільки, незважаючи на успіхи сучасної імунотерапії раку із застосуванням молекул інгібіторів імунних контрольних точок (Immune Checkpoint Inhibitors) вони демонструє обмежену ефективність від до 10 до 20%, що недостатньо, враховуючи їх вартість від $156000 до $257000 курс. На думку авторів дослідження, є можливість підвищити ефективність імунотерапії і зробити її доступною для мільйонів пацієнтів. Для цього створено інноваційний гомеопатичний препарат Меркурід, молекули якого є модулятором активності 4 білків мішеней PD-1/PD-L1, CD19, CD25, CD38, що зумовлює більшу ефективність у порівнянні з препаратами інгібіторами тільки 1 білка мішені PD1 або PD-L1.
Информация об авторе.
Артёмов Александр Валентинович, кандидат медицинских наук, заведующий лабораторией патологической анатомии и консервации тканей ГУ «Институт глазных болезней и тканевой терапии им. В.П. Филатова, НАМНУ» в. Одессе. Имеет более 120 публикаций. Бурячковский Эдуард Станиславович, кандидат медицинских наук, доцент кафедры патологической анатомии, декан международного факультета Одесского национального медицинского университета; автор более чем 75 работ. Лукьянчук Олег Валерьевич, главный врач ОООД, заслуженный врач Украины, заведующий кафедрой реконструктивной и восстановительной медицины с курсом репродуктологии, кандидат медицинских наук, доцент, врач высшей категории по специальности «Организация и управление здравоохранением», магистр государственного управления, врач-онкогинеколог высшей категории, главный внештатный онколог областного управления охраны здоровья и социальной защиты населения Одесской областной государственной администрации; автор более чем 100 публикаций. Врач Сергей Николаевич Гусев, кандидат медицинских наук, участник и дипломант международных профессиональных форумов, автор более 70 публикаций. Систематически проводит научные изыскания с коллегами, в рамках доказательной медицины. Патенты на молекулы и способы лечения принадлежат НИЦ "Меркурид", Украина, Одесса, ул. Старопортофранковская 101. Тел. +38 0482 320210.
Web-site: www.mercurid.com
E-mail: mercurid@te.net.ua
|
|||||||
Медицинский портал о гомеопатии и гомеопатах, в Одессе и мире. Прочтете все про лечение гомеопатией! Найдете центр гомеопатии. Гомеопатия аптека и гомеопатия форум. Гомеопатия в Украине
|
||||||||